Хлорид лития (Lithium chloride) увеличил мышечную силу и размер мышц у мышиных моделей с конечностно-поясной мышечной дистрофией D1 (КПМД D1, DNAJB6-связанная), блокируя белок, который чрезмерно вырабатывается у людей с этим типом КПМД.
В статье, написанной по результатам доклинического исследования Lithium chloride corrects weakness and myopathology in a preclinical model of LGMD1D, учёные делают предположение, что сдерживание (ингибирование) белка, чрезмерно вырабатываемого организмом при КПМД D1, может быть способом коррекции мышечной слабости у пациентов с этим видом конечностно-поясной мышечной дистрофии. Статья была опубликована в журнале Neurology Genetics.
В 2012 году исследовательская группа, возглавляемая Conrad C. Weihl (учёные степени MD и PhD, работает в Washington University School of Medicine in St. Louis), обнаружила, что изменения в гене DNAJB6 были причиной возникновения КПМД D1, которая приводит к прогрессирующему мышечному истощению с началом заболевания как в детском, так и во взрослом возрасте.
Учёные выявили две семьи, в которых у нескольких членов были симптомы КПМД, однако не была определена генетическая причина. Анализируя ДНК здоровых и заболевших членов семьи, учёные выяснили, что мутации в гене DNAJB6 были причиной мышечной слабости.
Несмотря на то, что дефектный ген был найден, не было ясно, почему изменения в этом гене вызывают мышечную атрофию.
Чтобы ответить на это, Weihl и соавторы Andrew Findlay (учёная степень MD) и Rocio Bengoechea (учёная степень PhD) создали мышиную модель с полностью отсутствующим геном DNAJB6.
Вопреки ожиданиям исследователей, вместо потери мышечной массы отсутствие гена DNAJB6 привело к разрастанию мышечных волокон в три раза больше их нормального размера.
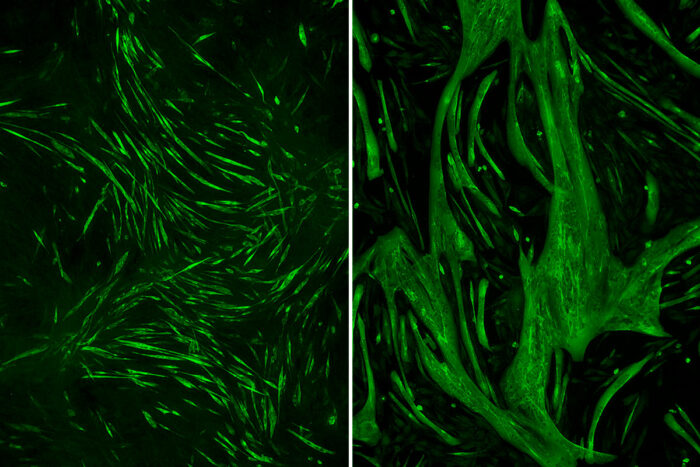
Для объяснения этой загадки исследователи изучали, что происходит с мышцами у мышей с такими же мутациями в гене DNAJB6, что и у людей, у которых была обнаружена КПМД D1. У мышей развивались симптомы прогрессирующей мышечной слабости во взрослом возрасте, так же как и у пациентов с этими мутациями.
Мышечные волокна мышей показали, что при таких генетических мутациях избыточно вырабатывается белок гликоген синтез киназа 3 бета (ГСК3β, glycogen synthase kinase 3 beta, GSK3β), который подавляет рост мышц. Когда исследователи блокировали этот белок у мышей с помощью хлорида лития, они увидели значительное восстановление силы и мышечной массы у мышей.
«До лечения мыши с мутацией обладали только 1/5 силы, которая должна быть у нормальной мыши», – говорит Findlay в пресс-релизе. – «После месяца лечения улучшения достигли 75% от нормального состояния мыши. Это большой шаг».
«Наши результаты свидетельствуют о том, что мутации в гене DNAJB6, ассоциированные с КПМД 1D, подавляют миогенные сигналы* из-за повышенной активности ГСК3β», – пишут исследователи.
*Примечание: миогенные сигналы – неточный перевод. В оригинале: “Our results suggest that LGMD1D-associated DNAJB6 mutations inhibit myogenic [muscle growth] signaling through augmented GSK3β activity”.
«Необходимы дальнейшие исследования, чтобы выяснить, является ли хлорид лития идеальным терапевтическим вариантом для лечения КПМД 1D».
Хлорид лития когда-то продавался в виде поваренной соли, однако был запрещён в 1940-х годах, когда врачи поняли, что его чрезмерное употребление может привести к летальному исходу. Другие формы лития (например, карбонат лития и цитрат лития) в настоящее время используются для лечения некоторых психиатрических заболеваний, поэтому возможно найти безопасную форму лития, которая может применяться для лечения этой редкой мышечной дистрофии, – говорится в пресс-релизе.
«Я не хочу, чтобы люди принимали хлорид лития прямо сейчас», – подчёркивает Findlay. «Мы показали, что белок представляет собой возможную терапевтическую мишень, но необходимо проделать большую работу».
Перед началом тестирования лечения, направленного на ГСК3β, исследователям необходимо лучше изучить природу КПМД. Эта болезнь настолько редкая, что не ясно, каким образом течение болезни и потеря мышечной силы варьируется среди людей с мутациями в разных генах.
«У нас есть терапевтическая мишень, но мы не до конца понимаем течение болезни у пациентов, которым не предоставляется лечение», – говорит Weihl.
Учёным необходимо как можно лучше понимать течение болезни, чтобы во время тестирования исследуемого препарата они могли быть уверены, что именно препарат меняет течение заболевания.
Weihl и Findlay вместе с коллегами из США и Соединённого Королевства в настоящее время планируют широкомасштабное исследование пациентов с КПМД с мутациями в любом гене с целью создания карты течения болезни. Такая карта будет иметь решающее значение для проведения клинических испытаний потенциального лечения.
Источники:
- Blocking Protein That Hinders Muscle Growth Possible Way of Treating LGMD1, Mouse Study Suggests
- Lithium chloride corrects weakness and myopathology in a preclinical model of LGMD1D
- Пресс-релиз Lithium boosts muscle strength in mice with rare muscular dystrophy на сайте Washington University School of Medicine in St. Louis и Medical Press
Внимание
Для сайта я подбираю материалы из различных источников, которые стараюсь максимально проверить на достоверность и научную значимость. Ссылки на источники размещаю в скобках после абзацев или в конце страницы/записи. Однако приведенную информацию нельзя рассматривать как абсолютно достоверный медицинский источник. Обязательно консультируйтесь со специалистами. Англо/франкоязычные тексты перевожу я сама. Я не врач. Если Вы нашли ошибку, неточность или хотите дополнить информацию, пожалуйста, напишите мне на электронную почту lgmd.ru@yandex.ru.
При использовании материалов сайта lgmd.ru обязательно указывайте активную ссылку на источник – сайт lgmd.ru.


Добавить комментарий